La corrosión es un proceso galvánico por el cual los metales se deterioran por oxidación, generalmente pero no siempre a sus óxidos. Por ejemplo, cuando se exponen al aire, el óxido de hierro, las manchas de plata y el cobre y el latón adquieren una superficie verde azulada llamada pátina. De los diversos metales sujetos a la corrosión, el hierro es, con mucho, el más importante comercialmente. Se estima que se gastan $ 100 mil millones por año solo en los Estados Unidos para reemplazar los objetos que contienen hierro destruidos por la corrosión. En consecuencia, el desarrollo de métodos para proteger las superficies metálicas de la corrosión constituye un área muy activa de investigación industrial. En esta sección, describimos algunos de los procesos químicos y electroquímicos responsables de la corrosión. También examinamos la base química de algunos métodos comunes para prevenir la corrosión y tratar metales corroídos.
La corrosión es un proceso REDOX.
En condiciones ambientales, la oxidación de la mayoría de los metales es termodinámicamente espontánea, con la notable excepción del oro y el platino. Por lo tanto, es realmente sorprendente que cualquier metal sea útil en absoluto en la atmósfera húmeda y rica en oxígeno de la Tierra. Sin embargo, algunos metales son resistentes a la corrosión por razones cinéticas. Por ejemplo, el aluminio en latas de refrescos y aviones está protegido por una fina capa de óxido metálico que se forma en la superficie del metal y actúa como una barrera impenetrable que evita una mayor destrucción. Las latas de aluminio también tienen una capa delgada de plástico para evitar la reacción del óxido con el ácido en el refresco. El cromo, el magnesio y el níquel también forman películas protectoras de óxido. Los aceros inoxidables son notablemente resistentes a la corrosión porque generalmente contienen una proporción significativa de cromo, níquel o ambos.
En contraste con estos metales, cuando el hierro se corroe, forma un óxido metálico hidratado rojo-marrón (Fe 2 O 3 • x H [19459015 ] 2 O), comúnmente conocido como óxido, que no proporciona una película protectora apretada (Figura ( PageIndex {1} )). En cambio, el óxido se desprende continuamente para exponer una superficie metálica fresca vulnerable a la reacción con oxígeno y agua. Debido a que se requiere oxígeno y agua para que se forme óxido, una uña de hierro sumergida en agua desoxigenada no se oxidará, incluso durante un período de varias semanas. Del mismo modo, una uña sumergida en un disolvente orgánico como el queroseno o el aceite mineral saturado con oxígeno no se oxidará debido a la ausencia de agua.
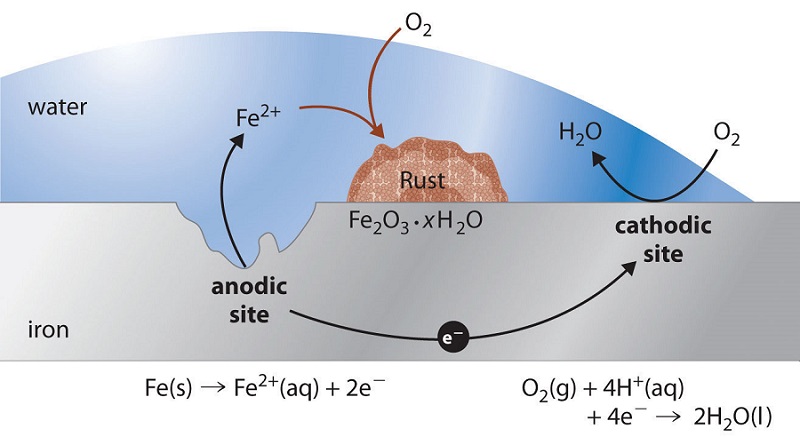
En el proceso de corrosión, el metal de hierro actúa como el ánodo en una celda galvánica y se oxida a Fe 2 + ; El oxígeno se reduce a agua en el cátodo. Las reacciones relevantes son las siguientes:
- en el cátodo: [O_ {2 (g)} + 4H ^ + _ {(aq)} + 4e ^ – rightarrow 2H_2O _ {(l)} ; ; ; E ° = 1.23 ; V label {Eq1} ]
- en el ánodo: [Fe {(s)} rightarrow Fe ^ {2 +} _ {(aq)} + 2e ^ – ; ; ; E ° = −0.45 ; V label {Eq2} ]
- global: [2Fe _ {(s)} + O_ {2 (g)} + 4H ^ + _ {(aq)} rightarrow 2Fe ^ {2 +} _ {(aq)} + 2H_2O _ {(l )} ; ; ; E ° = 1.68 ; V label {Eq3} ]
Los iones Fe 2 + producidos en la reacción inicial son oxidados por el oxígeno atmosférico para producir el óxido hidratado insoluble que contiene Fe 3 + , como se representa en la siguiente ecuación:
[4Fe ^ {2 +} _ {(aq)} + O_ {2 (g)} + (2 + 4x) H_2O rightarrow 2Fe_2O_3 cdot xH_2O + 4H ^ + _ {(aq)} label {Eq4} ]
El signo y la magnitud de E ° para el proceso de corrosión (Ecuación ( ref {Eq3} )) indican que existe una fuerte fuerza impulsora para la oxidación del hierro por O 2 según el estándar condiciones (1 MH + ). En condiciones neutras, la fuerza motriz es algo menor pero aún apreciable (E = 1.25 V a pH 7.0). Normalmente, la reacción del CO atmosférico 2 con agua para formar H + y HCO 3 – proporciona un pH lo suficientemente bajo como para mejorar el velocidad de reacción, al igual que la lluvia ácida. Los fabricantes de automóviles gastan una gran cantidad de tiempo y dinero desarrollando pinturas que se adhieren firmemente a la superficie metálica del automóvil para evitar que el agua oxigenada, el ácido y la sal entren en contacto con el metal subyacente. Desafortunadamente, incluso la mejor pintura está sujeta a arañazos o abolladuras, y la naturaleza electroquímica del proceso de corrosión significa que dos rasguños relativamente remotos entre sí pueden funcionar juntos como ánodo y cátodo, lo que lleva a una falla mecánica repentina (Figura ( PageIndex { 2} )).
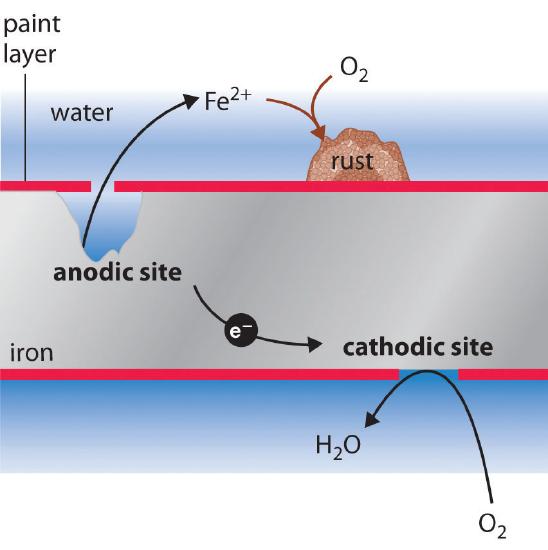
Protección profiláctica
Una de las técnicas más comunes utilizadas para prevenir la corrosión del hierro es aplicar una capa protectora de otro metal que es más difícil de oxidar. Los grifos y algunas partes externas de los automóviles, por ejemplo, a menudo se recubren con una fina capa de cromo mediante un proceso electrolítico. Sin embargo, con el mayor uso de materiales poliméricos en los automóviles, el uso de acero cromado ha disminuido en los últimos años. Del mismo modo, las “latas” que contienen sopas y otros alimentos en realidad están hechas de acero recubierto con una fina capa de estaño. Ni el cromo ni el estaño son intrínsecamente resistentes a la corrosión, pero ambos forman revestimientos protectores de óxido.

Al igual que con una pintura protectora, rascar un recubrimiento metálico protector permitirá que se produzca corrosión. Sin embargo, en este caso, la presencia del segundo metal puede aumentar la velocidad de corrosión. Los valores de los potenciales de electrodo estándar para Sn 2 + (E ° = −0,14 V) y Fe 2 + (E ° = −0,45 V) en La tabla P2 muestra que el Fe se oxida más fácilmente que el Sn. Como resultado, el metal más resistente a la corrosión (en este caso, el estaño) acelera la corrosión del hierro al actuar como el cátodo y proporcionar una gran área superficial para la reducción de oxígeno (Figura ( PageIndex {3} )) . Este proceso se observa en algunas casas antiguas donde las tuberías de cobre y hierro se han conectado directamente entre sí. El cobre oxidado con menos facilidad actúa como el cátodo, haciendo que el hierro se disuelva rápidamente cerca de la conexión y ocasionalmente resulte en una falla catastrófica de la tubería.
Protección catódica
Una forma de evitar estos problemas es usar un metal que se oxida más fácilmente para proteger el hierro de la corrosión. En este enfoque, llamado protección catódica, un metal más reactivo como Zn (E ° = −0.76 V para Zn 2 + + 2e – → Zn) se convierte en el ánodo, y el hierro se convierte en el cátodo. Esto evita la oxidación del hierro y protege el objeto de hierro de la corrosión. Las reacciones que ocurren en estas condiciones son las siguientes:
[ underbrace {O_ {2 (g)} + 4e ^ – + 4H ^ + _ {(aq)} rightarrow 2H_2O _ {(l)}} _ { text {reducción en el cátodo}} label {Eq5} ]
[ underbrace {Zn _ {(s)} rightarrow Zn ^ {2 +} _ {(aq)} + 2e ^ -} _ { text {oxidación en el ánodo}} label {Eq6} ]
[ underbrace {2Zn _ {(s)} + O_ {2 (g)} + 4H ^ + _ {(aq)} rightarrow 2Zn ^ {2 +} _ {(aq)} + 2H_2O _ {( l)}} _ { text {general}} label {Eq7} ]
El metal más reactivo reacciona con el oxígeno y eventualmente se disolverá, “sacrificándose” para proteger el objeto de hierro. La protección catódica es el principio subyacente del acero galvanizado, que es acero protegido por una fina capa de zinc. El acero galvanizado se usa en objetos que van desde clavos hasta botes de basura.

En una estrategia similar, los electrodos de sacrificio que usan magnesio, por ejemplo, se usan para proteger tanques o tuberías subterráneas (Figura ( PageIndex {4} )). Reemplazar los electrodos de sacrificio es más rentable que reemplazar los objetos de hierro que protegen.
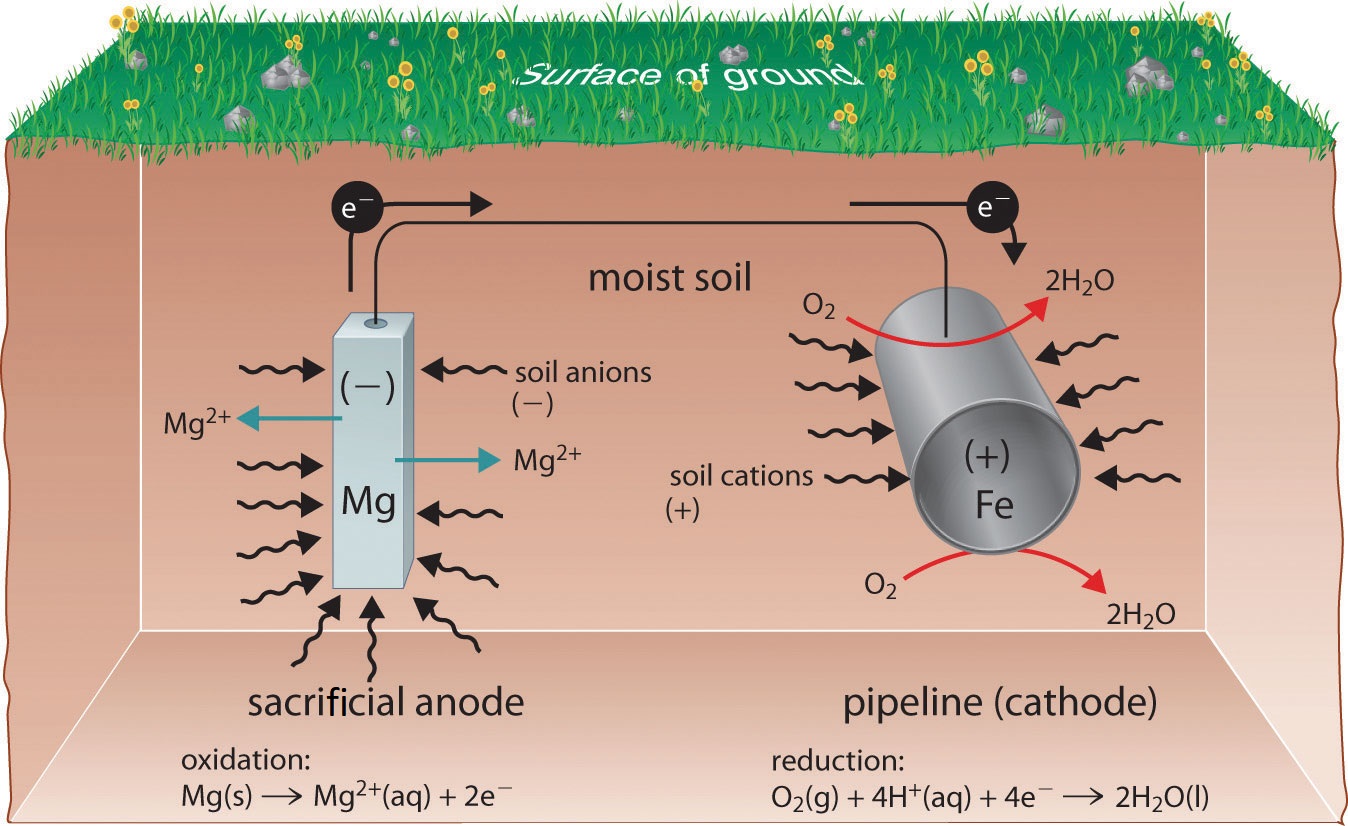
Resumen
La corrosión es un proceso galvánico que puede evitarse utilizando protección catódica. El deterioro de los metales a través de la oxidación es un proceso galvánico llamado corrosión. Los recubrimientos protectores consisten en un segundo metal que es más difícil de oxidar que el metal que se protege. Alternativamente, se puede aplicar un metal oxidado más fácilmente a una superficie metálica, proporcionando así una protección catódica de la superficie. Una fina capa de zinc protege el acero galvanizado. Los electrodos de sacrificio también se pueden unir a un objeto para protegerlo.