Los catalizadores son sustancias que aumentan la velocidad de reacción de una reacción química sin ser consumidos en el proceso. Por lo tanto, un catalizador no aparece en la estequiometría general de la reacción que cataliza, pero debe aparecer en al menos una de las reacciones elementales en el mecanismo de la reacción catalizada. La vía catalizada tiene una E a más baja, pero el cambio neto en la energía que resulta de la reacción (la diferencia entre la energía de los reactivos y la energía de los productos) no es afectado por la presencia de un catalizador ( Figur e ( PageIndex {1} )). Sin embargo, debido a su menor E a , la velocidad de reacción de una reacción catalizada es más rápida que la velocidad de reacción de la reacción no catalizada a la misma temperatura. Debido a que un catalizador disminuye la altura de la barrera de energía, su presencia aumenta las velocidades de reacción de las reacciones directas e inversas en la misma cantidad. En esta sección, examinaremos las tres clases principales de catalizadores: catalizadores heterogéneos, catalizadores homogéneos y enzimas.
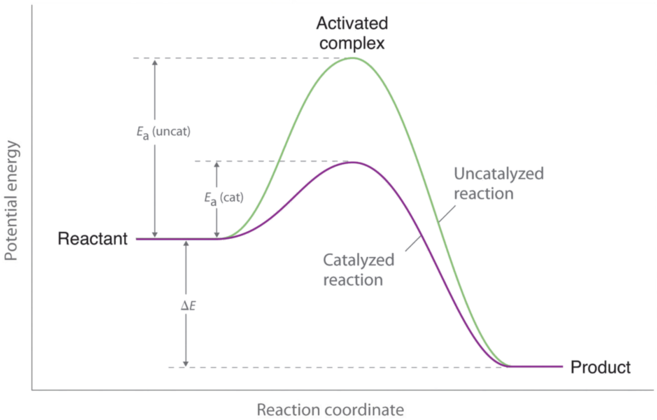
Un catalizador afecta a E a , no a Δ E .
Catálisis heterogénea
En catálisis heterogénea , el catalizador está en una fase diferente de los reactivos. Al menos uno de los reactivos interactúa con la superficie sólida en un proceso físico llamado adsorción de tal manera que un enlace químico en el reactivo se debilita y luego se rompe. Los venenos son sustancias que se unen irreversiblemente a los catalizadores, evitando que los reactivos se adsorban y, por lo tanto, reducen o destruyen la eficiencia del catalizador.
Un ejemplo de catálisis heterogénea es la interacción del hidrógeno gaseoso con la superficie de un metal, como Ni, Pd o Pt. Como se muestra en la parte (a) en Figura ( PageIndex {2} ) , los enlaces hidrógeno-hidrógeno se rompen y producen átomos de hidrógeno adsorbidos individuales en la superficie del metal. Debido a que los átomos adsorbidos pueden moverse en la superficie, dos átomos de hidrógeno pueden colisionar y formar una molécula de gas hidrógeno que luego puede salir de la superficie en el proceso inverso, llamado desorción. Los átomos de H adsorbidos en una superficie metálica son sustancialmente más reactivos que una molécula de hidrógeno. Debido a que el enlace H-H relativamente fuerte (energía de disociación = 432 kJ / mol) ya se ha roto, la barrera energética para la mayoría de las reacciones de H 2 es sustancialmente menor en la superficie del catalizador.
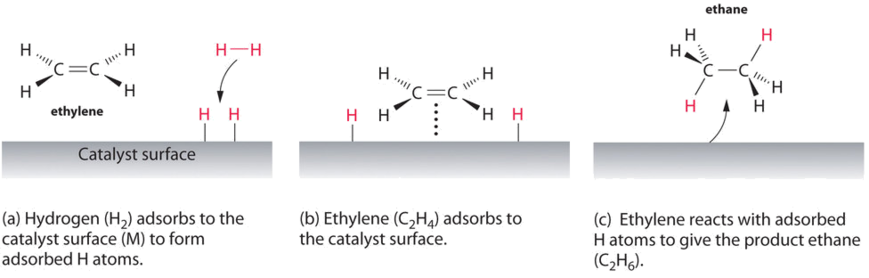
La figura ( PageIndex {2} ) muestra un proceso llamado hidrogenación , en el que se agregan átomos de hidrógeno al doble enlace de un alqueno, como el etileno, para dé un producto que contenga enlaces simples C – C, en este caso etano. La hidrogenación se usa en la industria alimentaria para convertir aceites vegetales, que consisten en largas cadenas de alquenos, en derivados sólidos más valiosos comercialmente que contienen cadenas de alquilo. La hidrogenación de algunos de los dobles enlaces en los aceites vegetales poliinsaturados, por ejemplo, produce margarina, un producto con un punto de fusión, textura y otras propiedades físicas similares a las de la mantequilla.
Varios ejemplos importantes de reacciones catalíticas heterogéneas industriales se encuentran en Tabla ( PageIndex {1} ). Aunque los mecanismos de estas reacciones son considerablemente más complejos que la simple reacción de hidrogenación descrita aquí, todos implican la adsorción de los reactivos en una superficie catalítica sólida, la reacción química de las especies adsorbidas (a veces a través de varias especies intermedias) y finalmente la desorción de los productos de la superficie.
| Proceso comercial | Catalizador | Reacción inicial | Producto comercial final |
|---|---|---|---|
| proceso de contacto | V 2 O 5 o Pt | 2SO 2 + O 2 → 2SO 3 | H 2 SO 4 |
| Proceso de Haber | Fe, K 2 O, Al 2 O 3 | N 2 + 3H 2 → 2NH 3 | NH 3 |
| Proceso de Ostwald | Pt y Rh | 4NH 3 + 5O 2 → 4NO + 6H 2 O | HNO 3 |
| reacción de cambio de agua-gas | Fe, Cr 2 O 3 o Cu | CO + H 2 O → CO 2 + H 2 | H 2 para NH 3 , CH 3 OH y otros combustibles |
| reforma de vapor | Ni | CH 4 + H 2 O → CO + 3H 2 | H 2 |
| síntesis de metanol | ZnO y Cr 2 O 3 | CO + 2H 2 → CH 3 OH | CH 3 OH |
| Proceso de Sohio | fosfomolibdato de bismuto | ( mathrm {CH} _2 textrm {= CHCH} _3 + mathrm {NH_3} + mathrm { frac {3} {2} O_2} rightarrow mathrm {CH_2} textrm {= CHCN} + mathrm {3H_2O} ) | ( underset { textrm {acrylonitrile}} { mathrm {CH_2} textrm {= CHCN}} ) |
| hidrogenación catalítica | Ni, Pd o Pt | RCH = CHR ′ + H2 → RCH 2 —CH 2 R ′ | aceites parcialmente hidrogenados para margarina, y así sucesivamente |
Catálisis homogénea
En catálisis homogénea , el catalizador está en la misma fase que el (los) reactivo (s). El número de colisiones entre los reactivos y el catalizador es máximo porque el catalizador se dispersa uniformemente por toda la mezcla de reacción. Muchos catalizadores homogéneos en la industria son compuestos de metales de transición ( Tabla ( PageIndex {2} )), pero la recuperación de estos costosos catalizadores de la solución ha sido un gran desafío. Como una barrera adicional para su uso comercial generalizado, muchos catalizadores homogéneos se pueden usar solo a temperaturas relativamente bajas, e incluso entonces tienden a descomponerse lentamente en solución. A pesar de estos problemas, se han desarrollado varios procesos comercialmente viables en los últimos años. El polietileno y el polipropileno de alta densidad se producen por catálisis homogénea.
| Proceso comercial | Catalizador | Reactantes | Producto final |
|---|---|---|---|
| Union Carbide | [Rh (CO) 2 I 2 ] – | CO + CH 3 OH | CH 3 CO 2 H |
| proceso de hidroperóxido | Complejos de Mo (VI) | CH 3 CH = CH 2 + R – O – O – H | 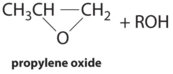 |
| hidroformilación | Rh / PR 3 complejos | RCH = CH 2 + CO + H 2 | RCH 2 CH 2 CHO |
| proceso de adiponitrilo | Ni / PR 3 complejos | 2HCN + CH 2 = CHCH = CH 2 | NCCH 2 CH 2 CH 2 CH 2 CN utilizado para sintetizar nylon |
| polimerización de olefinas | (RC 5 H 5 ) 2 ZrCl 2 | CH 2 = CH 2 | – (CH 2 CH 2 -) n : polietileno de alta densidad |
Enzimas
Las enzimas, catalizadores que ocurren naturalmente en los organismos vivos, son casi todas moléculas de proteínas con masas moleculares típicas de 20,000–100,000 amu. Algunos son catalizadores homogéneos que reaccionan en solución acuosa dentro de un compartimento celular de un organismo. Otros son catalizadores heterogéneos incrustados dentro de las membranas que separan las células y los compartimentos celulares de su entorno. El reactivo en una reacción catalizada por enzimas se denomina sustrato .
Debido a que las enzimas pueden aumentar la velocidad de reacción por factores enormes (hasta 10 17 veces la velocidad no catalizada) y tienden a ser muy específicas, por lo general producen un solo producto con rendimiento cuantitativo, son el foco de investigación activa Al mismo tiempo, las enzimas suelen ser caras de obtener, a menudo dejan de funcionar a temperaturas superiores a 37 ° C, tienen una estabilidad limitada en la solución y tienen una especificidad tan alta que se limitan a convertir un conjunto particular de reactivos en un producto en particular . Esto significa que se deben desarrollar procesos separados que usen diferentes enzimas para reacciones químicamente similares, lo que lleva mucho tiempo y es costoso. Hasta ahora, las enzimas han encontrado solo aplicaciones industriales limitadas, aunque se usan como ingredientes en detergentes para ropa, limpiadores de lentes de contacto y ablandadores de carne. Las enzimas en estas aplicaciones tienden a ser proteasas, que pueden escindir los enlaces amida que mantienen unidos los aminoácidos en las proteínas. Los ablandadores de carne, por ejemplo, contienen una proteasa llamada papaína, que se aísla del jugo de papaya. Escinde algunas de las largas y fibrosas moléculas de proteína que hacen que los cortes de carne de res sean económicos y duros, produciendo un trozo de carne que es más tierno. Algunos insectos, como el escarabajo bombardero, llevan una enzima capaz de catalizar la descomposición del peróxido de hidrógeno en agua ( Figura ( PageIndex {3} )).

Los inhibidores de la enzima causan una disminución en la velocidad de reacción de una reacción catalizada por enzimas al unirse a una porción específica de una enzima y, por lo tanto, ralentizar o evitar que ocurra una reacción. Los inhibidores irreversibles son, por lo tanto, el equivalente de venenos en catálisis heterogénea. Uno de los inhibidores de enzimas comerciales más antiguos y más utilizados es la aspirina, que inhibe selectivamente una de las enzimas involucradas en la síntesis de moléculas que desencadenan la inflamación. El diseño y la síntesis de moléculas relacionadas que son más efectivas, más selectivas y menos tóxicas que la aspirina son objetivos importantes de la investigación biomédica.
Resumen
Los catalizadores participan en una reacción química y aumentan su velocidad. No aparecen en la ecuación neta de la reacción y no se consumen durante la reacción. Los catalizadores permiten que una reacción proceda a través de una vía que tiene una energía de activación menor que la reacción no catalizada. En la catálisis heterogénea, los catalizadores proporcionan una superficie a la que los reactivos se unen en un proceso de adsorción. En catálisis homogénea, los catalizadores están en la misma fase que los reactivos. Las enzimas son catalizadores biológicos que producen grandes aumentos en las velocidades de reacción y tienden a ser específicos para ciertos reactivos y productos. El reactivo en una reacción catalizada por enzimas se llama sustrato. Los inhibidores de la enzima causan una disminución en la velocidad de reacción de una reacción catalizada por enzimas.