Las leyes que describen el comportamiento de los gases estaban bien establecidas mucho antes de que alguien hubiera desarrollado un modelo coherente de las propiedades de los gases. En esta sección, presentamos una teoría que describe por qué los gases se comportan como lo hacen. La teoría que presentamos también se puede utilizar para derivar leyes como la ley del gas ideal a partir de principios fundamentales y las propiedades de partículas individuales.
Una descripción molecular
La teoría cinética molecular de los gases explica las leyes que describen el comportamiento de los gases. Desarrollado a mediados del siglo XIX por varios físicos, incluido el austríaco Ludwig Boltzmann (1844–1906), el alemán Rudolf Clausius (1822–1888) y el inglés James Clerk Maxwell (1831–1879), también conocido por su Esta teoría, basada en las contribuciones a la electricidad y al magnetismo, se basa en las propiedades de las partículas individuales definidas para un gas ideal y los conceptos fundamentales de la física. Así, la teoría cinética molecular de los gases proporciona una explicación molecular para las observaciones que condujeron al desarrollo de la ley de los gases ideales. La teoría cinética molecular de los gases se basa en los siguientes cinco postulados:
Aunque las moléculas de gases reales tienen volúmenes distintos de cero y ejercen fuerzas atractivas y repulsivas entre sí, por el momento nos centraremos en cómo la teoría molecular cinética de los gases se relaciona con las propiedades de los gases que hemos estado discutiendo. En las siguientes secciones, explicamos cómo debe modificarse esta teoría para tener en cuenta el comportamiento de los gases reales.
Los postulados 1 y 4 afirman que las moléculas de gas están en constante movimiento y chocan frecuentemente con las paredes de sus contenedores. La colisión de moléculas con sus paredes de contenedor da como resultado una transferencia de impulso (impulso) de las moléculas a las paredes (Figura ( PageIndex {2} )).
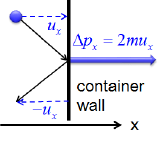
La transferencia de momento a la pared perpendicular al eje (x ) como una molécula con una velocidad inicial (u_x ) en (x ) golpes de dirección se expresa como:
[ Delta p_x = 2mu_x label {10.7.1} ]
La frecuencia de colisión , una cantidad de colisiones de las moléculas a la pared por unidad de área y por segundo, aumenta con la velocidad molecular y el número de moléculas por unidad de volumen.
[f propto (u_x) times Big ( dfrac {N} {V} Big) label {10.7.2} ]
La presión que ejerce el gas sobre la pared se expresa como el producto del impulso y la frecuencia de colisión.
[P propto (2mu_x) times (u_x) times Big ( dfrac {N} {V} Big) propto Big ( dfrac {N} {V} Big) mu_x ^ 2 label {10.7.3} ]
Sin embargo, en cualquier instante, las moléculas en una muestra de gas viajan a diferente velocidad. Por lo tanto, debemos reemplazar (u_x ^ 2 ) en la expresión anterior con el valor promedio de (u_x ^ 2 ), que se denota por ( overline {u_x ^ 2} ). La barra superior designa el valor promedio sobre todas las moléculas.
La expresión exacta para la presión se da como:
[P = dfrac {N} {V} m overline {u_x ^ 2} label {10.7.4} ]
Finalmente, debemos considerar que no hay nada especial en la dirección (x ). Deberíamos esperar que
[ overline {u_x ^ 2} = overline {u_y ^ 2} = overline {u_z ^ 2} = dfrac {1} {3} overline {u ^ 2}. ]
Aquí la cantidad ( overline {u ^ 2} ) se llama velocidad cuadrática media definida como el valor promedio de la velocidad cuadrada ( (u ^ 2 )) sobre todo moléculas. Desde
[u ^ 2 = u_x ^ 2 + u_y ^ 2 + u_z ^ 2 ]
para cada molécula, luego
[ overline {u ^ 2} = overline {u_x ^ 2} + overline {u_y ^ 2} + overline {u_z ^ 2}. ]
Al sustituir ( dfrac {1} {3} overline {u ^ 2} ) por ( overline {u_x ^ 2} ) en la expresión anterior, podemos obtener la expresión final para la presión :
[P = dfrac {1} {3} dfrac {N} {V} m overline {u ^ 2} label {10.7.5} ]
Debido a que los volúmenes y las interacciones intermoleculares son insignificantes, los postulados 2 y 3 afirman que todas las partículas gaseosas se comportan de manera idéntica, independientemente de la naturaleza química de sus moléculas componentes. Esta es la esencia de la ley de los gases ideales, que trata todos los gases como colecciones de partículas que son idénticas en todos los aspectos, excepto la masa. El postulado 2 también explica por qué es relativamente fácil comprimir un gas; simplemente disminuyes la distancia entre las moléculas de gas.
El Postulado 5 proporciona una explicación molecular de la temperatura de un gas. El postulado 5 se refiere al promedio traslacional energía cinética de las moléculas de un gas (( overline {e_K}) ), que puede representarse como y afirma que a una temperatura Kelvin dada ((T) ) , todos los gases tienen el mismo valor de
[ overline {e_K} = dfrac {1} {2} m overline {u ^ 2} = dfrac {3} {2} dfrac {R} {N_A} T label {10.7. 6} ]
donde (N_A ) es la constante de Avogadro. La energía cinética traslacional total de 1 mol de moléculas se puede obtener multiplicando la ecuación por (N_A ):
[N_A overline {e_K} = dfrac {1} {2} M overline {u ^ 2} = dfrac {3} {2} RT label {10.7.7} ]
donde (M ) es la masa molar de las moléculas de gas y está relacionada con la masa molecular por (M = N_Am ). Al reorganizar la ecuación, podemos obtener la relación entre la velocidad cuadrática media raíz ( (u _ { rm rms} )) y la temperatura. La velocidad rms ( (u _ { rm rms} )) es la raíz cuadrada de la suma de las velocidades cuadradas dividida por el número de partículas:
[u _ { rm rms} = sqrt { overline {u ^ 2}} = sqrt { dfrac {u_1 ^ 2 + u_2 ^ 2 + cdots u_N ^ 2} {N}} label {10.7.8} ]
donde (N ) es el número de partículas y (u_i ) es la velocidad de la partícula (i ).
La relación entre (u _ { rm rms} ) y la temperatura viene dada por:
[u _ { rm rms} = sqrt { dfrac {3RT} {M}} label {10.7.9} ]
En la ecuación ( ref {10.7.9} ), (u _ { rm rms} ) tiene unidades de metros por segundo; en consecuencia, las unidades de masa molar (M ) son kilogramos por mol, la temperatura (T ) se expresa en grados Kelvin y la constante de gas ideal (R ) tiene el valor 8.3145 J / (K • mol). La ecuación ( ref {10.7.9} ) muestra que (u _ { rm rms} ) de un gas es proporcional a la raíz cuadrada de su temperatura Kelvin e inversamente proporcional a la raíz cuadrada de su masa molar. La velocidad cuadrática media de un gas aumenta con el aumento de la temperatura. A una temperatura dada, las moléculas de gas más pesadas tienen velocidades más lentas que las más livianas.
La velocidad eficaz y la velocidad promedio no difieren mucho (generalmente en menos del 10%). Sin embargo, la distinción es importante porque la velocidad eficaz es la velocidad de una partícula de gas que tiene una energía cinética promedio. Las partículas de diferentes gases a la misma temperatura tienen la misma energía cinética promedio, no la misma velocidad promedio. En contraste, la velocidad más probable (vp) es la velocidad a la que se mueve la mayor cantidad de partículas. Si la energía cinética promedio de las partículas de un gas aumenta linealmente con el aumento de la temperatura, entonces la ecuación ( ref {10.7.8} ) nos dice que la velocidad eficaz también debe aumentar con la temperatura porque la masa de las partículas es constante. Por lo tanto, a temperaturas más altas, las moléculas de un gas se mueven más rápidamente que a temperaturas más bajas, y aumenta vp.
A una temperatura dada, todas las partículas gaseosas tienen la misma energía cinética promedio pero no la misma velocidad promedio.
Distribuciones de Boltzmann
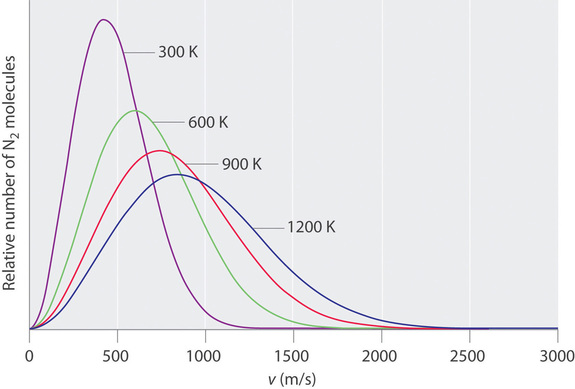
En cualquier momento, ¿qué fracción de las moléculas en una muestra particular tiene una velocidad dada? Algunas de las moléculas se moverán más lentamente que el promedio, y algunas se moverán más rápido que el promedio, pero ¿cuántas en cada situación? Las respuestas a preguntas como estas pueden tener un efecto sustancial en la cantidad de producto formado durante una reacción química. Este problema fue resuelto matemáticamente por Maxwell en 1866; Utilizó el análisis estadístico para obtener una ecuación que describe la distribución de velocidades moleculares a una temperatura dada. Las curvas típicas que muestran las distribuciones de velocidades de las moléculas a varias temperaturas se muestran en la Figura ( PageIndex {3} ). El aumento de la temperatura tiene dos efectos. Primero, el pico de la curva se mueve hacia la derecha porque aumenta la velocidad más probable. En segundo lugar, la curva se ensancha debido a la mayor difusión de las velocidades. Por lo tanto, el aumento de la temperatura aumenta el valor de la velocidad más probable, pero disminuye el número relativo de moléculas que tienen esa velocidad. Aunque las matemáticas detrás de las curvas como las de la Figura ( PageIndex {3} ) fueron desarrolladas por primera vez por Maxwell, las curvas se denominan casi universalmente como Distribuciones de Boltzmann , después de una de las otras figuras principales responsable de la teoría cinética molecular de los gases.
Las relaciones entre presión, volumen y temperatura
Ahora describimos cómo la teoría cinética molecular de los gases explica algunas de las relaciones importantes que hemos discutido anteriormente.
- Presión versus volumen : a temperatura constante, la energía cinética de las moléculas de un gas y, por lo tanto, la velocidad eficaz no cambian. Si se permite que una muestra de gas determinada ocupe un volumen mayor, entonces la velocidad de las moléculas no cambia, pero la densidad del gas (número de partículas por unidad de volumen) disminuye y la distancia promedio entre las moléculas aumenta. Por lo tanto, las moléculas deben, en promedio, viajar más lejos entre colisiones. Por lo tanto, chocan entre sí y con las paredes de sus contenedores con menos frecuencia, lo que lleva a una disminución de la presión. Por el contrario, aumentar la presión obliga a las moléculas a estar más juntas y aumenta la densidad, hasta que el impacto colectivo de las colisiones de las moléculas con las paredes del recipiente simplemente equilibra la presión aplicada.
- Volumen versus temperatura : elevar la temperatura de un gas aumenta la energía cinética promedio y, por lo tanto, la velocidad eficaz (y la velocidad promedio) de las moléculas de gas. Por lo tanto, a medida que aumenta la temperatura, las moléculas chocan con las paredes de sus contenedores con mayor frecuencia y con mayor fuerza. Esto aumenta la presión, a menos que el volumen aumente para reducir la presión, como acabamos de ver. Por lo tanto, un aumento en la temperatura debe compensarse con un aumento en el volumen para que el impacto neto (presión) de las moléculas de gas en las paredes del recipiente permanezca sin cambios.
- Presión de mezclas de gases : El postulado 3 de la teoría cinética molecular de los gases establece que las moléculas de gas no ejercen fuerzas atractivas o repulsivas entre sí. Si las moléculas gaseosas no interactúan, la presencia de un gas en una mezcla de gases no tendrá efecto sobre la presión ejercida por otro, y la ley de Dalton de presiones parciales se mantiene.
Resumen
- La teoría cinética molecular de los gases proporciona una explicación molecular de las observaciones que condujeron al desarrollo de la ley de los gases ideales.
- Energía cinética promedio: [ overline {e_K} = dfrac {1} {2} m {u _ { rm rms}} ^ 2 = dfrac {3} {2} dfrac {R} {N_A} T no número ]
- Velocidad cuadrática media raíz: [u _ { rm rms} = sqrt { dfrac {u_1 ^ 2 + u_2 ^ 2 + cdots u_N ^ 2} {N}}
onumber ] - Teoría cinética molecular de los gases: [u _ { rm rms} = sqrt { dfrac {3RT} {M}}
onumber ]
El comportamiento de los gases ideales se explica por la teoría cinética molecular de los gases . El movimiento molecular, que conduce a colisiones entre las moléculas y las paredes del recipiente, explica la presión, y las grandes distancias intermoleculares en los gases explican su alta compresibilidad. Aunque todos los gases tienen la misma energía cinética promedio a una temperatura dada, no todos poseen la misma velocidad cuadrática media (rms) [ v rms [ 19459026] ) . Los valores reales de velocidad y energía cinética no son los mismos para todas las partículas de un gas, pero están dados por una distribución de Boltzmann , en la que algunas moléculas tienen velocidades (y energías cinéticas) más altas o más bajas que el promedio.